 | ||
특히 오리엔탈제약의 “콜키퍼캅셀”의 경우 PPA를 전면 금지키로 한 보고서가 식약청에 제출된 이후에 허가된 것으로 밝혀졌다.
식약청이 국회 전재희 의원(한나라당, 경기 광명을)에게 제출한 자료에 따르면, 이번에 제조,판매가 금지된 166개의 저용량 PPA 함유 의약품(1일 최대 복용량 100밀리그램 이하) 중 13개 품목이 식약청이 2001년 7월 25일 페닐프로판올아민 함유제제 안전대책을 통해 뇌졸중 위험성에 역학조사를 실시하기로 결정한 이후에 허가된 것으로 나타났다.
 | ||
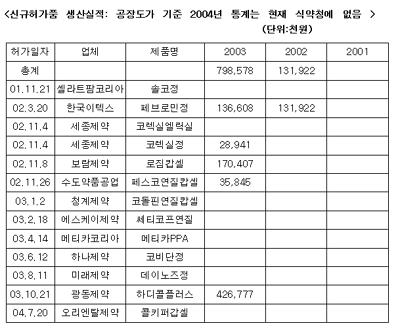
▷2001년 11월 21일: 쎌라트팜코리아/ 솔코정
▷2002년 3월20일: 한국이텍스/페브로민정
- 11월 4일: 세종제약/코렉실엘릭실
11월 4일: 세종제약/코렉실정
- 11월 8일: 보람제약/로짐캅셉
-11월 26일: 수도약품공업/페스코 연질캅셀
▷2003년
- 1월 2일: 청계제약/코돌핀 연질캅셀
- 2월 18일: 에스케이제약/쎄티코프 연질캅셀
- 4월14일: 메디카코리아/메디카염산페닐프로판올아민(원료)
- 6월12일: 하나제약/코비단정
- 8월11일: 미래제약/데이노즈정
- 10월 21일: 광동제약/하디콜플러스정
▷2004년
- 7월20일:오리엔탈제약/콜키퍼캅셀
이중 오리엔탈제약의 “콜키퍼캅셀”은 6월 25일 용량에 관계없이 모든 PPA 제품을 전면 제조.금지키로 한 근거자료인 서울대 연구팀의 최종보고서가 식약청에 제출된 이후인 7월 20일에 품목허가가 나 충격을 주고 있다.
전 의원은 한쪽에서는 치명적인 질병을 유발할 위험성이 있다며 역학조사를 실시하면서, 다른 한쪽에서는 허가를 남발하여 국민들의 건강을 위협하고 있었다고 주장했다.
이와관련 식약청은 기존제품이 아직 판매금지되기 전이어서 “형평성”(?) 때문에 허가를 내 줄 수 밖에 없었다고 주장한 것으로 알려졌다.
전재희 의원은 “ 판매금지를 하지 않은 이유가 위험성이 입증되지 않았기 때문이라면, 상당한 위험성이 예상되어 역학조사를 실시하고 있는 의약품에 대해 안전성이 입증되기 전에는 신규허가를 억제하고 안정성이 확인될 때까지 신중하게 관리하는 것이 위험한 의약품 관리의 원칙”이라고 말했다.

